世界初 植物の根の内部構造を決める起動スイッチの働きを三次元で解明
世界初 植物の根の内部構造を決める起動スイッチの働きを三次元で解明
水が通る維管束や内皮、表皮の作り分けを巧みに調節
~根の生長促進などバイオマスの生産性向上に期待~
奈良先端科学技術大学院大学(奈良先端大 学長:小笠原直毅)バイオサイエンス研究科の箱嶋敏雄教授、平野良憲助教、村瀬浩司助教らの研究グループは米国デューク大学との共同研究により、植物(シロイヌナズナ)の根の内部構造を決める起動スイッチとして働く2つのタンパク質=SHORT-ROOT(SHR)とSCARECROW(SCR)=が、遺伝情報読み取りの目印になるタグを識別するタンパク質 =JACKDAW(JKD)(※1)=とともに形成する三者複合体の立体的なかたちを、X線結晶構造解析法(※2)という手法を使って可視化することに世界で初めて成功した。これにより、3つのタンパク質が共同して根の基本的な内部構造(内側から維管束、内皮、皮層、表皮)を形作っていくために必要な遺伝情報を複数の遺伝子DNAから読み取る機構が明らかになった。
平野 良憲助教のコメント
SHORT-ROOT (SHR)、SCARECROW (SCR)は
SHR、SCRはGRASファミリーという大きな転写制御ファミリーの一員で、GRASファミリーは植物ホルモン“ジベレリン”シグナルや豆の根粒形成など、様々なシグナル伝達経路に関与しています。本成果で明らかとなったGRASファミリーの基本的な分子機能は、このような他のシグナル伝達経路での機能解明も加速することが期待されます。
本成果は当研究室修了生の中川雅啓君、須山友絵さんと共に長い時間を費やした成果です。放射光施設SPring-8で、一緒に一喜一憂ながら深夜まで実験したことを昨日のように思い出します。彼らの惜しみない努力に感謝します。また、共同研究者の先生方にも深く感謝申し上げます。
【概要】
奈良先端科学技術大学院大学(奈良先端大 学長:小笠原直毅)バイオサイエンス研究科の箱嶋敏雄教授、平野良憲助教、村瀬浩司助教らの研究グループは米国デューク大学との共同研究により、植物(シロイヌナズナ)の根の内部構造を決める起動スイッチとして働く2つのタンパク質=SHORT-ROOT(SHR)とSCARECROW(SCR)=が、遺伝情報読み取りの目印になるタグを識別するタンパク質 =JACKDAW(JKD)(※1)=とともに形成する三者複合体の立体的なかたちを、X線結晶構造解析法(※2)という手法を使って可視化することに世界で初めて成功した。これにより、3つのタンパク質が共同して根の基本的な内部構造(内側から維管束、内皮、皮層、表皮)を形作っていくために必要な遺伝情報を複数の遺伝子DNAから読み取る機構が明らかになった。
構造解析の結果、SHRとSCRは1対1で結合して複合体を形成しており、その複合体のSHRの凹んだ溝にJKDがはまり込んでいることから、JKDの特徴的なアミノ酸の配列がSHRによって識別されていることが明らかとなり、この識別されるアミノ酸の配列を「SHR結合モチーフ」と命名した。
JKDは遺伝子DNAに直接結合してどの遺伝子情報を読み取る位置を決める「転写因子」(※3)であり、JKDとよく似た転写因子は16種類あり、総称してBIRDファミリーと呼ばれている。今回の研究では、この中の13種が「SHR結合モチーフ」をもっており、SHR-SCR複合体と結合することがわかった。こうしたことから、これらの相互作用を通してSHR-SCR複合体が、複数の転写因子からなるネットワークを活性化することで、根に特有な内部構造を形成するために必要な多くのタンパク質をつくるという分子メカニズムが解明された。つまり、これらの働きにより、根の中心に水や養分の通る維管束、内皮を挟んで外側に皮層や表皮が作り分けられるという根の基本構造形成の仕組みがつきとめられた。
今回の成果に基づいて、根の成長促進や改良等の品種改良の研究が進み、農作物やバイオマスの生産性向上などにつながると期待される。
本成果は、英科学誌 Nature の植物専門オンライン姉妹誌、Nature Plants(3 月号)に掲載される(プレス解禁日時:日本時間 平成 29 年 2 月 18 日(土曜日)午前 1 時)/ロンドン時間平成 29 年 2 月 17 日(金曜日)午後 4 時)。
【掲載論文】
論文タイトル:Structure of the SHR-SCR heterodimer bound to the BIRD/IDD transcriptional factor JKD
(和訳:BIRD/IDD型転写因子JKDに結合したSHR-SCRヘテロ二量体の構造)
著者:Yoshinori Hirano 1, Masahiro Nakagawa 1, Tomoe Suyama 1, Kohji Murase 1, 2, Maya Shirakawa 1,Seiji Takayama 2,3, Tai-ping Sun 4 and Toshio Hakoshima 1*
所属:1,2 奈良先端科学技術大学院大学,3 東京大学,4 Duke University
掲載論文:Nature Plants(3月号)
【背景】
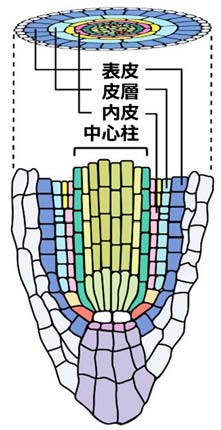
図1 根の内部構造
動物や植物などの生き物は、多数の細胞からできているが、それらの細胞は集合するだけではなく、ある決まった構造を自ら生み出して、特定の役割を担う部位や器官や臓器を形成している。植物では、地上部に花、葉、茎があり、地中には、根が張り巡らされている。植物の根は、成長に必須な水や養分を取り込んで植物体内へ運んだり、植物体を固定したりする重要な役割をもっている。毒性物質への耐性に優れた根や、大地にしっかり張り巡らされた強い根への改良は、重金属や酸性土や塩害等の汚染、あるいは台風や豪雨等の災害に強い作物等の作出を可能にする。
植物の根を拡大してみると、いくつかの組織からなることが分かっており、各組織が目的にあった役割を担っている(図1)。根の中心部には「中心柱」と呼ばれる組織があり、そこには維管束等が通っており、水や養分の通り道となっている。その外側には「内皮」と呼ばれる層があり、これより外側は皮層や表皮が形成されており、中心柱を守っている。このような放射状の基本的な内部構造パターンがどうしてできるかは植物学にとって解き明かすべき根本的な問題であった。
【解説】
これまでの研究から上記の放射状の内部構造パターン形成を制御する遺伝子は幾つか見つかっていた。それらの中で最も重要なのは、これらの遺伝子から作られるSHRとSCRと呼ばれる2つのタンパク質であることがわかってきた。SHRとSCRは、植物特有のGRASファミリーと呼ばれるタンパク質であり、様々な解析により、遺伝子からの遺伝情報を写し取る(転写)活性を上昇させる因子であると推測されていた。さらに、SHRは中心柱で作られるが、SCRは中心柱の外側で作られていることが分かっている。また、SHRは細胞や組織中を移動するタンパク質であるが、SCRは移動しない。中心柱で作られたSHRが外側へ拡散していき、SCRと出会ったところで、互いに相互作用し合い、更に、他の必要なタンパク質とも相互作用し合って、その部位の形成に必要な遺伝子を活性化して、中心柱を囲む内皮や皮層の細胞への分化を開始すると考えられていた(図2)。
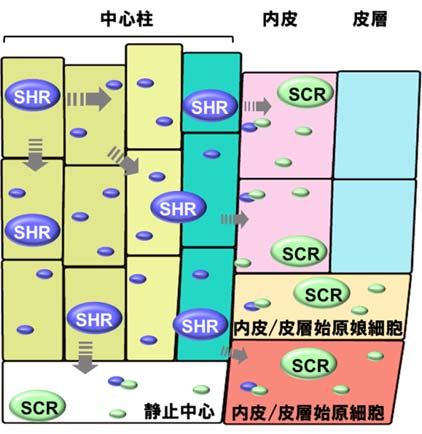
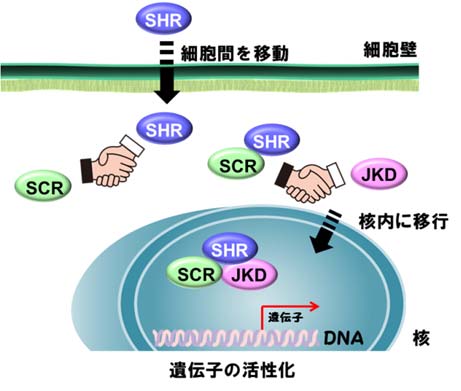
図2.移動するSHRと移動しないSCRとの出会いとJKDによる遺伝子の活性化
【研究成果】

図3.SHRとSCRタンパク質複合体の結晶
「SHRとSCRはどのようにして互いを認識するのか?」
本研究では、SHRとSCRのタンパク質を実験室でつくり、相互作用を調べた。すると、この2つが1対1で固く結合して、安定な複合体を形成することがわかった。そこで、この複合体を単離して結晶化を試みた。その結果、美しい結晶(図3)を得ることが出来たので、兵庫県播磨の大型放射光施設SPring-8でこの結晶にX線を照射して回折データを収集した。そのデータを持ち帰り、X線結晶構造解析を行って、SHR-SCR複合体の三次元構造を決定することに成功した。
SHRとSCRはよく似た構造をしており、互いに相補的な分子表面をもち、しっかり張り付いて、双子のように対をなしていた(図4の左図)。驚いたことに、これらの構造は、よく知られていたメチル化酵素と類似した構造をもっていることが判明した。しかし、構造を詳しく調べてみると、メチル化酵素の活性に必要な補酵素の結合部位がないなどのことがわかり、メチル化酵素としては働いていないことがわかった。このように、本来ある機能をもつタンパク質が、その機能とは関連のない他の機能にも使い回されるようになったものは、「ハイジャックタンパク質」として知られている。これは進化の過程で、既に存在していたタンパク質が流用されて、新しい役割を持つようになったと考えられている。SHRとSCRの場合は、遺伝子の活性化(転写の活性化)という新しい機能が進化の過程で付与された。
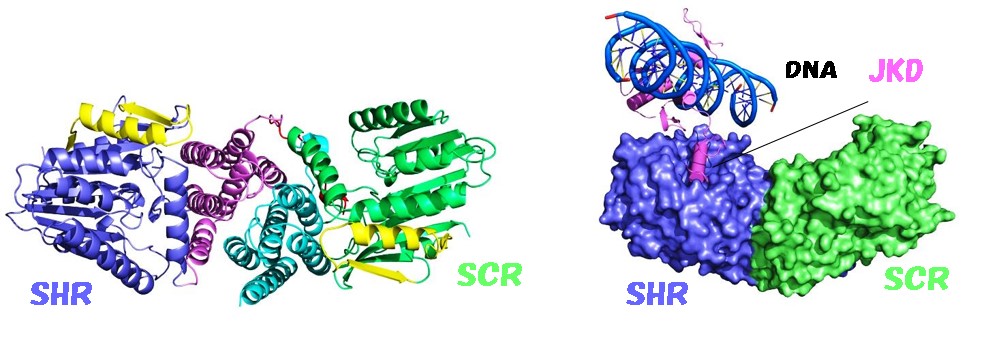
図4. SHR-SCR 複合体およびJKD-SHR-SCR三者複合体の立体構造
左図:SHRとSCRの二者複合体の構造。
右図: JKD-SHR-SCR三者複合体の構造。JKDのZFはSHRの溝にはまり込む一方、DNAとも同時に相互作用する(DNAはモデル)。
「SHRとSCRはどのようにして活性化すべき遺伝子を選別するのか?」
SHRとSCRが遺伝子を活性化することは知られていたが、そのためには、活性化しなければならない目的遺伝子DNAと相互作用することで、その遺伝子を巨大な染色体の中から見つけてこなければならない。ところが、SHR-SCRの構造をも調べてみても、DNAと相互作用する領域は見当たらない。実際、実験してみても、直接のDNAへの結合は観測されなかった。DNAと直接に相互作用して、どの遺伝子がどこにあるかを見つけ出すタンパク質として転写因子(※3)と呼ばれる一群のタンパク質が知られている。これらの中で、JACKDAW(JKD)とMAGPIE(MGP)が、SHRとSCRの経路で働いているらしいことが分かってきた。そこで、転写因子JKDやMGPとSHR-SCR複合体との相互作用を実験的に解析してみた。すると、JKDやMGPのもつDNA結合部位近辺とSHR-SCR複合体とが直接に相互作用することを突き止めた。次に、SHR-SCR複合体にJKDを結合させて三者複合体として、これを結晶化した。この結晶を用いてX線結晶解析を行い、三者複合体の三次元構造の詳細を明らかにした。この構造から、SHRの分子表面には特徴的な溝があり、そこにJKDのDNA結合部位の一部がはまり込み、その部分のアミノ酸配列を識別されていることがわかった(図4の右図)。
より詳細に解析すると、JKDはDNAと直接に相互作用してDNAの塩基配列を読みとることが知られているジンクフィンガー(ZF、※4)と呼ばれる塩基配列読み取り装置を持ち、それは4つ(ZF1、ZF2、ZF3、ZF4)あるが、これらの中で、JKD分子のN末端側のZF1、ZF2、ZF3の3つはDNAの塩基配列の読み取りに、C末端側のZF3とZF4の2つはSHRと相互作用することが判明した。特に、ZF4がSHRの凹んだ溝にはまり込んで、そのアミノ酸配列が識別される。この識別されるアミノ酸配列を、「SHR結合モチーフ」("SHR-binding motif, SHBM")と命名した。
また、JKDとよく似た転写因子は16種類あり、総称してBIRDファミリーの転写因子と呼ばれているが、この中の13種が「SHR結合モチーフ」をもっており、SHR-SCR複合体と結合することがわかった。これら13の転写因子は、それぞれ別々の遺伝子を識別していると考えられるので、SHR-SCR複合体が、SHR結合モチーフの識別を通して、複数のBIRDファミリーの転写因子を必要な遺伝子の目印のDNAタグ識別タンパク質として利用することで、一群の遺伝子発現を根の生長に応じて活性化する「遺伝子ネットワーク起動スイッチ」として働くという分子メカニズムが解明された(図5)。
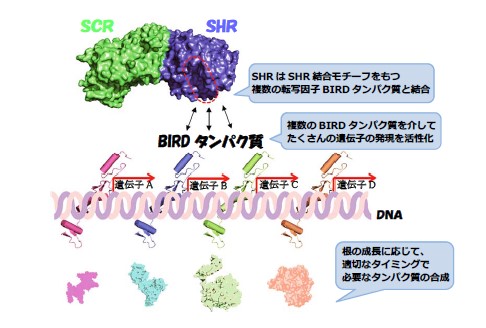
図5.SHR、SCRとBIRDタンパク質による転写制御メカニズム
【今後の展開】
本成果は、根の発達を制御する複雑な転写制御メカニズムの一端を原子レベルで明らかにしたもので、この知見を基盤として、根の成長制御メカニズムの全容解明に向けたさらなる研究が進展するとともに、根の成長を人為的に操作することで農作物の品種改良や植物バイオマスの増産に向けた試みが加速していくものと期待される。
【用語解説】
※1 タンパク質の名前:
SHR(SHORT-ROOT) 短い根
SCR(SCARECROW) かかし
JDK(JACKDAW) ニシコクマルガラス(西黒丸ガラス)
MGP(MAGPIE) カササギ
BIRDファミリー転写因子 鳥の名前が付けられた転写因子群からなるファミリー
※2 X線結晶構造解析法:光の回折現象を応用して、X 線を結晶に照射して得られる回折パターンから結晶中の分子の立体的な配置を決定する方法。結晶が得られるとタンパク質やDNAなどの複雑な生体高分子から構成される複合体の立体構造を原子レベルで決定することができる。兵庫県にある大型放射光施設 SPring-8 といった、強力なエネルギーをもつシンクロトロンでの放射 X 線を用いることで微小な結晶(0.01 - 0.5 mm程度)からデータを収集することができる。
※3 転写因子:生物の設計図に相当する遺伝子を構成するDNAの特定の領域に直接結合して、遺伝情報を写し取るスピードを調節するスイッチとして働くタンパク質の総称。DNAの遺伝情報はメッセンジャーRNAに写し取られ(転写)、この情報が翻訳されてリボソームという合成装置でタンパク質が合成される。転写因子は数多く存在して、それぞれ標的とする遺伝子が異なっており、また転写因子の遺伝子も別な転写因子によって調節を受けているため、複雑な転写調節ネットワークが形成されている。
※4 ジンクフィンガー:タンパク質にみられる亜鉛イオンと結合する構造モチーフ。システインまたはヒスチジンが亜鉛イオンとの結合に使われ、結合した亜鉛はタンパク質の構造を安定化する働きをしている。DNAと結合して、その塩基配列読み取る装置として発見されたが、現在ではRNAやタンパク質と相互作用することもあることが分かっている。
研究室紹介ページ:http://bsw3.naist.jp/courses/courses306.html
研究室ホームページ:http://bsw3.naist.jp/hako/
(2017年03月01日掲載)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学