植物代謝制御 (出村研究室)
-
研究室ホームページ
- https://bsw3.naist.jp/demura/
-
全学オンラインセミナー
2022年度に開催されたBio Discovery Session(全学オンラインセミナー)のアーカイブ動画の一覧です。 - Bio Discovery Session
-
Webメディア
NAIST Edge BIOは、奈良先端科学技術大学院大学 バイオサイエンス領域 の各研究室で取り組んでいる「最先端」の研究プロジェクトや研究成果について、研究者だけではなく受験生や一般の方にも分かりやすく紹介するためのWebメディアです。 - NAIST Edge BIO 第13回
主な研究テーマ
有用バイオマス植物の開発
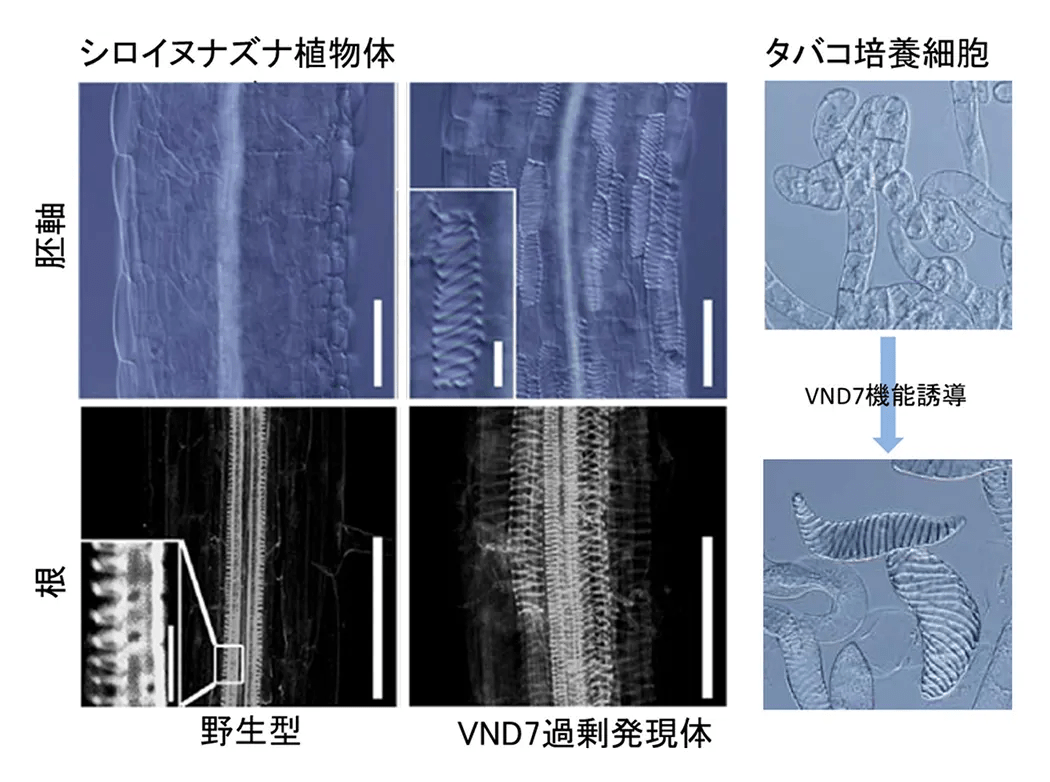
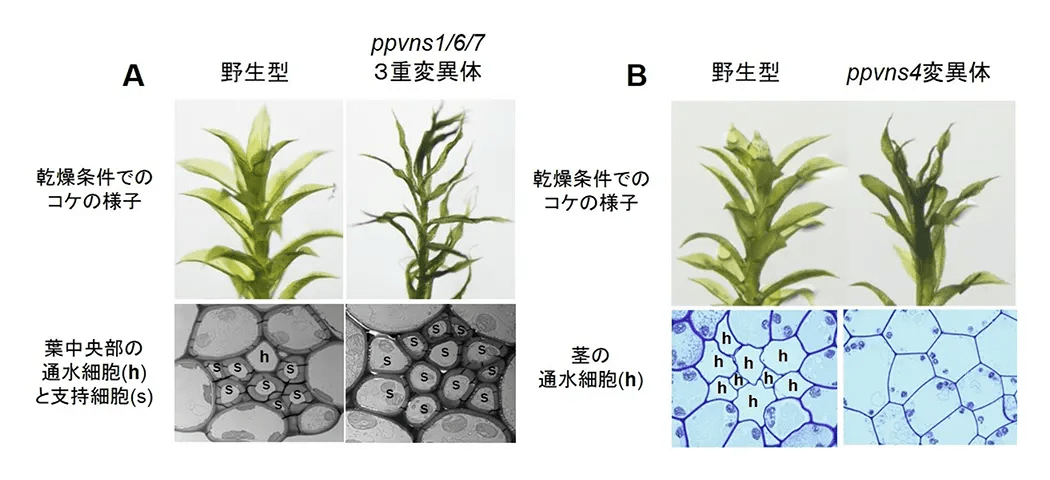
様々なモデル研究システム(シロイヌナズナや培養細胞)を用いて、木質バイオマスを構成する木質細胞の分化を制御するしくみの解明に取り組んでいます。とくに、オミクス(ゲノム、トランスクリプトーム、プロテオーム、メタボローム)情報をベースにした統合的な解析により、木質細胞の一種である道管細胞の分化や、木質バイオマスの本体である植物細胞壁の生合成を制御する遺伝子の発見に成功しています(図1)。木質バイオマスを改良したモデル樹木の開発や(図2)、コケ植物などの多様な植物種を用いた進化発生的研究にも取り組んでいます(図3)。これらを通じ、有用バイオマス植物作出に向けた汎用性の高い基盤技術の開発研究を推進しています。
植物の力学的最適化メカニズムに基づく基盤技術の開発
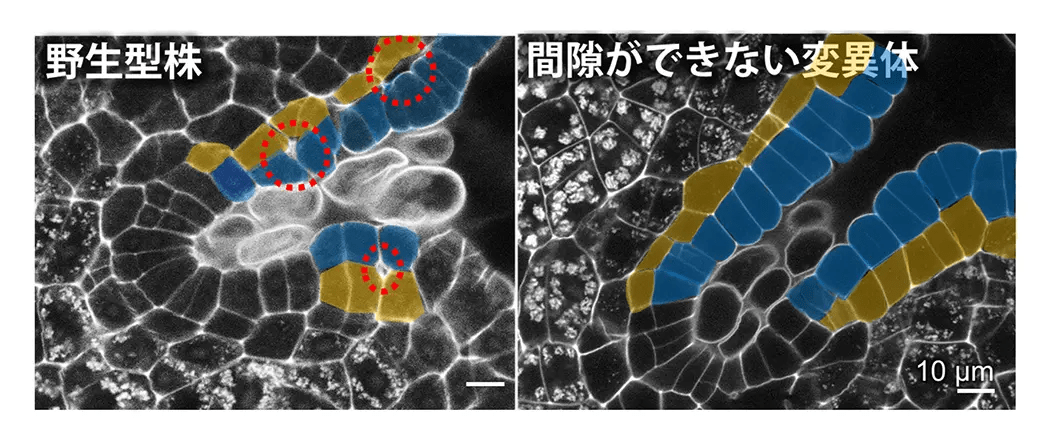
植物は発生や環境応答の過程で自らの身体構造を力学的に最適な形へと変化させています。この植物の力学的最適化システムを、さまざまなスケール(生体分子−細胞−組織−個体)で解析(図4)し、そのメカニズムの解明を進めています。原子間力顕微鏡AFMを用いた力学特性解析や、タイムラプスカメラ・マイクロX線CT・IoT機器(Raspberry Piなど)を用いた3D・4D構造特性解析、これらと数理解析を組み合わせた構造力学解析に取り組んでいます。得られた研究成果をもとに、植物の高機能化といった次世代バイオ基盤技術の確立をはじめ、地震や台風、四季の温度差など日本という国土固有の多様な環境因子に調和したサステナブル建築への応用展開を目指しています。
自発光植物の社会実装に向けた基盤技術の開発
自発光キノコなどの発光生物がもつ生物発光システムを植物に導入(遺伝子組換え)することで、自発光する植物を作出することができます。当研究室では、大阪大学永井健治教授との共同研究として、自発光ポプラの作出に成功しています(図5)。今後、自発光植物を照明として利用するなどの社会実装のためには、発光強度の増強などのさらなる機能改変が必要です。すでに、発光強度の増強を目指した研究として、外的に薬剤刺激を与える方法や、特定の時期や特定の細胞に自発光を限定する方法の開発に取り組んでいます。これらを通じ、自発光植物の社会実装を目指します。
主な発表論文・著作
- Miyake A. et al., Curr. Biol., 36, 1086-1095, 2026
- Koyama T. et al., New Phytol., 248, 2981-2995, 2025
- Kunieda T. et al., Electronics Comm. Japan, 107, e12448, 2024
- Phookaew P. et al., Plant Cell, 36, 3298-3317, 2024
- Takahara M. et al., Plant Physiol., 192, 857-870, 2023
- Nakano Y. et al., Front. Plant Sci., 13, 819360, 2022
- Hirai R. et al., Front. Plant Sci., 13, 825810, 2022
- Akiyoshi N. et al., Plant Cell Physiol., 62, 1963-1974, 2021
- Terada et al., Plant Mol. Biol., 106, 309-317, 2021
- Nakata M.T. et al., Front. Plant Sci., 12, p654655, 2021
- Ramachandran V. et al., Plant Mol Biol, 104, 263-281, 2020
- Yoneda A. et al., Plants, 9, 604, 2020
- Tsugawa S. et al., Plant Biotechnol, 37, 443-450, 2020
- Kunieda T. et al., Plant Biotechnol, 37, 465-469, 2020
- Nakata M.T. et al., Plant Biotechnol, 37, 471-474, 2020
- Kunieda T. et al., Plant Cell Physiol., 61, 308-317, 2020
- Akiyoshi N. et al., Tree Physiol., 40, 704-716, 2020
- Tamura T. et al., Plant J., 100, 298-313, 2019
- Kubo M. et al., Nucleic Acids Res., 47, 4539-4553, 2019
- Ohtani M. et al., Curr. Opin. Biotech, 56, 82-87, 2019
- Takenaka Y. et al., Plant Cell, 30, 2663-2676, 2018
- Noguchi M. et al., Plant Biotechnol, 35, 31-37, 2018
- Tan T. et al., Plant Physiol, 176, 773-789, 2018
- Xu B. et al., Science, 343, 1505-1508, 2014
(こちらのリンクはすべて外部サイトへ遷移します![]() )
)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学