血液中の肺がん遺伝子異常を調べる高感度技術を開発、承認申請へ 超高速の次世代遺伝子解析を使い、微細な変化を検出 ~患者に優しい遺伝子検査でがんの精密医療を推進する~
血液中の肺がん遺伝子異常を調べる高感度技術を開発、承認申請へ
超高速の次世代遺伝子解析を使い、微細な変化を検出
~患者に優しい遺伝子検査でがんの精密医療を推進する~
【概要】
奈良先端科学技術大学院大学(学長:横矢直和)先端科学技術研究科 バイオサイエンス領域 疾患ゲノム医学研究室の加藤菊也特任教授は大阪国際がんセンターの呼吸器内科、呼吸器外科との共同研究により、血液中に存在する微量の肺がん遺伝子の異常(変異)を検出する高感度技術を開発しました。株式会社DNAチップ研究所が7月10日に厚生労働省へ本技術(製品名 EGFRリキッド遺伝子解析ソフトウェア、略称 EGFRリキッド)の承認申請を行います。承認されれば、医療現場で使用することができます。
イレッサなどの上皮成長因子受容体(EGFR)のチロシンキナーゼを阻害する薬剤は、進行性肺がん治療に広く使われているのですが、その効果はEGFR遺伝子に特定の変異がある場合に限られるため、これらの変異の検出が薬剤を選択する際の条件になっています。日本ではEGFR変異陽性肺がんは約半数と多く、年間5万件以上のEGFR遺伝子検査が行われています。
一般にがんの遺伝子検査では生検(検査のためがん組織を採取する操作)でがん組織を取得する必要がありますが、患者の苦痛を伴い、また人体への侵襲が問題になるケースがあります。しかし、がん患者の血液中には肺がん細胞から放出されたEGFR遺伝子があり、これを解析すれば、患者の負担を軽減したうえで変異を検出することが可能です。このような血液を用いたがん遺伝子検査はリキッドバイオプシーとよばれ、現在世界中で盛んに研究開発が行われています。
今回、開発した技術は、次世代シークエンシング(強力な遺伝子解析技術で個人の全遺伝情報の取得も可能)の手法を用いて血液中のEGFR遺伝子を5万分子以上解析して変異を探索します。そのため、従来技術では検出できなかった微量変異でも検出可能です。
こうした"精密医療"は遺伝子異常に基づいて治療法を決定する新しい医療コンセプトで、米国のオバマ前大統領が一般教書演説で取り上げて注目を浴びました。本技術は日本における精密医療を大幅に加速すると予想されます。なお国内研究の実用化はリキッドバイオプシーとしては初めて、次世代シークエンシングを使う手法としてはがん遺伝子検査「OncoGuide™ NCCオンコパネルシステム(国立がん研究センター・シスメックス)」に次いで2件目です。
加藤菊也特任教授のコメント

今回のプレスリリースの研究内容は論文としては6年前(2013年)の発表です。しかしながら医療技術の科学的評価は論文発表では終結せず、厚生労働省の承認を得て初めて完結することになります。これまで大規模な臨床試験や本技術に関する各種性能試験を行い、ようやく承認申請にこぎつけました。実用化という点ではまだ道半ばですが、広く医療現場で使われるまで研究開発を続けます。
【解説】
1.背景と目的
イレッサ、タルセバ等の上皮成長因子受容体チロシンキナーゼ阻害剤(EGFR-TKI)は、EGFRに活性化変異(exon 19 deletion、L858Rなど)がある非小細胞肺がん(肺がん患者の90%以上を占める)患者にのみ効果がある。そのためEGFR変異検査は進行肺がん治療に必須であり、このような治療の前に薬剤を選択するための遺伝子検査をコンパニオン診断と呼ぶ。検査のためには肺生検でがん組織を採取するが、肺がんは他臓器のがんに比べて腫瘍組織の採取が難しく、侵襲性が高い。またEGFR-TKI治療により耐性がおこるが、その約半数はEGFRの別の変異(T790M耐性変異)による。病態モニタリングや耐性変異用EGFR-TKI選択のため耐性変異検査のニーズが高いが、再発巣や転移巣の生検はさらに難しい。こうしたことから、非侵襲で行えるEGFR変異検査の研究開発が2005年頃から行われてきており、本開発もその流れを汲んでいる。
EGFR検査を非侵襲性の血液検査で代替できれば、この領域の実地臨床に大きな進歩をもたらすことになる。がん患者血液中にはがん細胞から遊離したDNA(circulating tumor DNA, ctDNA)が極少量存在し、EGFRの変異を検出できる。但しctDNAは極微量しか含まれていないため、検出は非常に難しい。微量変異を検出する技術の開発が必須であった。
2.技術の原理及び性能の検証
次世代シークエンシング技術(NGS)は遺伝情報を解析する強力な技術で、個人の全ゲノム配列(全遺伝情報)でも低コストで得ることができる。個人の全ゲノムを解析する代わりに肺がん患者血液中のEGFR遺伝子断片のみを多数(実際には5万分子以上)解析して変異を探索すれば、変異が低頻度でも検出することが可能である。従来の検査技術では5%の変異がないと検出できないが、今回は例えば1万分子解析すれば0.01%の変異でも検出できる。加藤特任教授=当時大阪府立成人病センター(現大阪国際がんセンター)研究所長=は2013年にこの検出技術を開発した。
新しい技術を開発しても実際に使えるかどうか肺がん患者で試験を行わなければならない。加藤特任教授と今村文生大阪国際がんセンター副院長(当時大阪府立成人病センター呼吸器内科主任部長)は288名の肺がん患者について従来の検査法(肺がん組織の生検)と新しい技術(血液を使用)を比較し、「十分実地臨床で使用可能」との成績を得た。この試験は2013-2015年に行った。
3.承認申請までの経緯
以上の研究成果を踏まえて、本技術の薬事承認申請をするために厚生労働省傘下の独立行政法人医薬品医療機器総合機構(PMDA)と協議を始めた。しかしながら当時は次世代シークエンサーの薬事行政上の取扱いが定まっておらず協議が難航した。徐々に次世代シークエンサーの医療上の重要性が一般にも理解されるようになり、厚生労働省の見解も定まってきた。
2017年からPMDAとの協議を再開し、本検出技術に関する追加データについて議論を行った。主要な追加実験は、同一検体(肺がん組織)を用いた従来法と本技術の比較である。2018年に奈良先端科学技術大学院大学と大阪国際がんセンター呼吸器外科の岡見次郎主任部長及び東山聖彦副院長との共同研究でこの比較試験を行い、良好な結果を得た。その他の申請に必要な各種データは株式会社DNAチップ研究所で取得、2019年3月のPMDAとの協議で、承認申請の了解を得た。正式な製品名称は以下のとおりである。
類別:プログラム1 疾病診断用プログラム
一般的名称:体細胞遺伝子変異解析プログラム(抗悪性腫瘍薬適応判定用)
販売名:EGFRリキッド遺伝子解析ソフトウェア
4.今後の展開
現在非小細胞肺がんではEGFR以外にALK ROS1 BRAFの3つの遺伝子に対応した薬剤があり、EGFR-TKI同様、それぞれの遺伝子の変異検出が薬剤選択の条件になっている。現在これらの遺伝子検査は別々に行われているが、次世代シークエンサーを用いれば同時に行うことができる。このような検査を一般に遺伝子検査パネルと呼び、この検査法が開発された米国ではすでに広く用いられている。しかしながら従来の遺伝子検査パネルは日本の肺がん医療現場での使用は難しい。米国と異なり日本では気管支鏡による生検が中心で、採取するがん組織の量が少ないためで、変異検出感度が重要になるが、これらの遺伝子検査パネルには十分な感度がない。
このような現状を打開すべく奈良先端科学技術大学院大学、大阪国際がんセンター、株式会社DNAチップ研究所の共同研究で高感度の遺伝子検査パネルを開発している。このパネルはEGFR ALK ROS1 BRAFの4つの遺伝子が対象で、2020年内に完成の予定である。なお、コストを抑えるため肺がん組織のみを対象としている(血液検体は扱わない)。
【用語解説】
1.上皮成長因子受容体チロシンキナーゼ阻害剤(EGFR-TKI):
EGFR-TKIは進行性非小細胞肺がんの治療に広く使われている薬剤である。治療効果がEGFR遺伝子に特定の変異(エクソン19欠失、L858Rなど)がある場合に限られるため、これらの変異の検出が薬剤選択の条件になっている。日本ではEGFR変異陽性の比率が50%以上で、年間5万件以上のEGFR遺伝子検査が行われている。
2.非小細胞肺がん:
最も多い肺がんで全肺がんの90%以上を占める。肺がんには非小細胞肺がん以外に小細胞肺がんや大細胞肺がんがある。
3.リキッドバイオプシー:
がん患者の血液中にはがん細胞から放出された遊離DNAがあり、高感度な検出技術を用いれば、この遊離DNAを用いて遺伝子検査をすることができる。血液を用いたがん遺伝子検査はリキッドバイオプシー(体液を用いた生検)とよばれ、生検の侵襲を回避するほか、がんの早期発見にも役立つ可能性があるため、現在世界中で盛んに研究開発が行われている。
4.次世代シークエンシング・次世代シークエンサー:
遺伝情報を解析する強力な技術で、個人の全ゲノム配列(全遺伝情報)でも低コストで得ることができる(現在一人当たり10万円)。EGFRリキッドでは全ゲノムを一回解析するかわりに、EGFR遺伝子のみを5万分子以上解析して変異を探索する。そのため目的の遺伝子変異が低頻度でも検出することが可能である。
5.コンパニオン診断:
EGFR-TKIに対応するEGFR遺伝子検査のように、特定薬剤選択の条件になっている遺伝子変異を検出する検査。
6.遺伝子検査パネル:
多数の遺伝子の異常を次世代シークエンサーで同時検出する検査。使用用途はコンパニオン診断とゲノムプロファイリングに大別される。ゲノムプロファイリングは標準治療の効かなくなった患者の治療方針決定の補助に用いられる。なお、国立がん研究センターの「OncoGuide™ NCCオンコパネルシステム」はゲノムプロファイリング専用でコンパニオン診断に用いることはできない。
【イメージ図】
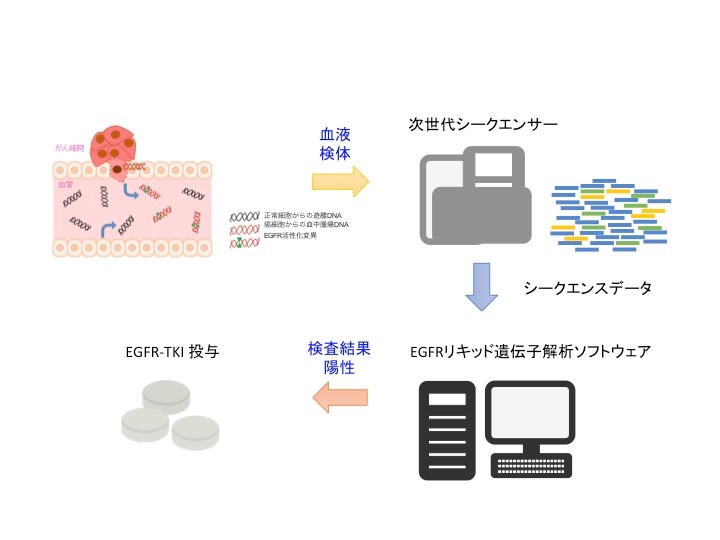
【文献】
Kukita, Y., Uchida, J., Oba, S., Nishino, K., Kumagai, T., Tanguchi, K., Okukyma, T., Imamura, F. and Kato, K. Quantitative identification of mutant alleles derived from lung cancer in plasma cell-free DNA via anomaly detection using deep sequencing data, PLoS ONE 8 (2013): e81468.
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0081468
Uchida, J., Kato, K., Kukita, Y., Kumagai, T., Nishino, K., Daga, H., Nagatomo, I., Inoue, T., Kimura, M., Oba, S., Ito, Y., Takeda, K. and Imamura, F. Diagnostic accuracy of noninvasive genotyping of EGFR in lung cancer patients using deep sequencing of plasma cell-free DNA. Clinical Chemistry, 51 (2015) 1191–1196.
http://clinchem.aaccjnls.org/content/61/9/1191
【疾患ゲノム医学研究室】
研究室紹介ページ:https://bsw3.naist.jp/courses/courses501.html
(2019年07月29日掲載)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学