2022.11.01
胚盤胞補完法により臓器を作るために必要な条件とは何か?
器官発生工学研究室・助教・由利 俊祐
- 要旨
- 現在、移植用臓器の不足を補うために、再生医療研究がさかんに行われています。しかし、複数種の細胞と複雑な三次元構造からなる臓器を生体外で再構築することは極めて難しいです。そこで、臓器欠損動物由来の初期胚 (胚盤胞) に多能性幹細胞を注入し、多能性幹細胞由来の臓器を動物体内に作製することができる「胚盤胞補完法」が注目されています。しかしながら、異種間キメラ動物を用いた胚盤胞補完法では、作製できる臓器とできない臓器があることが知られており、胚盤胞補完法による臓器の作製のために必要な条件は不明なままでいました。本稿では、これまでの自身の研究により、胚盤胞補完法で臓器を作るために必要な条件が分かってきましたので、その研究と今後解決していくべき課題について紹介していきます。
- 主要関連論文
- Generation of rat lungs by blastocyst complementation in Fgfr2b-deficient mouse model
Shunsuke Yuri, Yuki Murase, Ayako Isotani
Biorxiv 2022
1.はじめに
2010年代初頭に、胚盤胞補完法技術を用いた異種臓器作成の成功が報告されたにもかかわらず、その後、異種キメラ動物を用いた胚盤胞補完法による臓器作出の成功はほとんど報告されていません。そこで、過去の文献からの課題、2017年に奈良先端科学技術大学院大学へ赴任して以降に行ってきた胚盤胞補完法に関わる研究成果、そして、今後について紹介します。
2.臓器移植の現状と胚盤胞補完法
臓器移植は、眼球、肺、心臓、肝臓、膵臓、腎臓、小腸で行われており、2021年に臓器移植を希望する人は国内で13,000人を超えていました。しかしながら、2021年に臓器移植を受けることができた人は125人しかおらず、移植用の臓器は絶対的に不足しています。 2006年にiPS細胞が樹立され1)、自身の“体細胞”を 体のすべての細胞になることができる“多能性幹細胞”へ転換し、生体外で望みの細胞を作ることが理論的に可能となりました。それ以来、iPS細胞を使った再生医療技術の開発はめざましいものがあります。機能する臓器を作るためには、臓器が持つ複雑な三次元的な構造を再現することが必要となりますが、生体外で臓器を作る際には、そのような構造を作ることは難しいのが現状です。そこで、この問題の解決方法として、動物体内で臓器を作らせることができる『胚盤胞補完法』が着目されています。『胚盤胞補完法』とは、特定の臓器を作ることができない動物の初期胚 (胚盤胞) へ多能性幹細胞を注入し、動物の体の中で多能性幹細胞由来の臓器を作り出す方法のことです (図1)。将来的には、臓器を作り出すことができない動物の胚盤胞へヒトのiPS細胞を注入することで、ヒトの臓器を動物体内で作り出すことが期待されています。
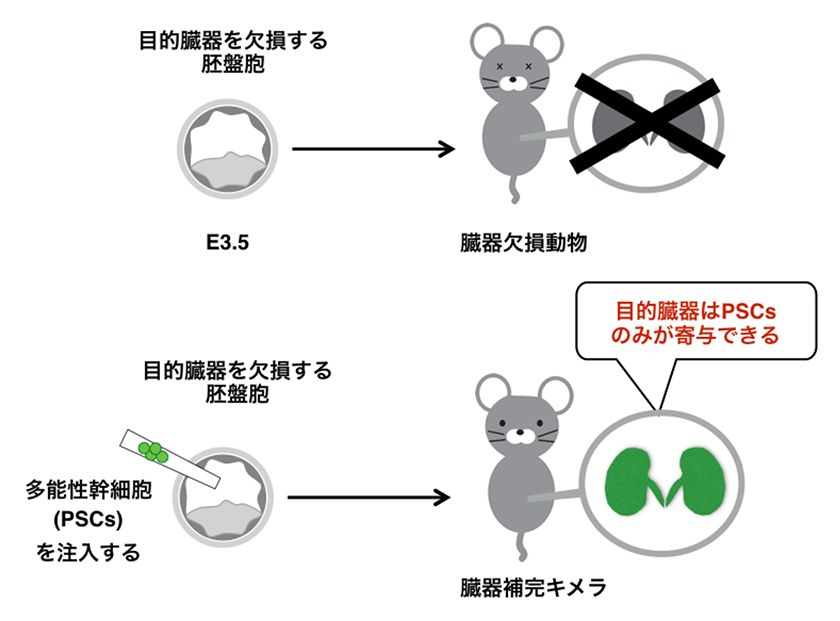
図1.胚盤胞補完法
目的臓器を欠損する胚盤胞は、そのまま発生すると臓器を欠損するが (上図)、そこへ多能性幹細胞を注入すると、多能性幹細胞は目的臓器へ分化することができるため、目的臓器は多能性幹細胞由来となる (下図)。
3.胚盤胞補完法の歴史とその問題点
胚盤胞補完法の最初の報告例は1993年で、T細胞やB細胞を産生できないRag2遺伝子の欠損動物の胚盤胞に野生型マウス胚性幹細胞(ES細胞)を注入した研究でした2)。この報告により、将来的に臓器や細胞が欠損する胚盤胞を作ることができれば、理論的には動物体内で多能性幹細胞由来の細胞や臓器を作り出すことができることが示唆されました。また、2010年には、膵臓欠損マウスの体内で機能的なラットの膵臓の作製3)、2011年には、当器官発生工学研究室の磯谷綾子准教授が、胸腺欠損マウス体内で機能的なラット胸腺を作り出すことにも成功しました4)。これらの報告により、異種間でも胚盤胞補完法を実施することが可能であることが示され、以降は、腎臓、心臓、眼球、肺、甲状腺、肝臓、骨、骨格筋、生殖細胞、脳など様々な臓器に対する胚盤胞補完法の報告が多く出されるようになりました。しかしながら、それらの研究の中で、同種間での胚盤胞補完法では、多能性幹細胞由来の臓器が作ることができるにもかかわらず、異種間では作り出すことができない臓器や組織があることがわかってきました。例えば、腎臓を欠損するマウスの胚盤胞にラットES細胞を補完した場合は、腎臓はラットに置き換わらずに腎臓ができないこと5)、血管や血球細胞を欠損するマウスの胚盤胞の場合も、ラット細胞が血管や血球細胞を補完することはありませんでした6)。一方で、腎臓を欠損するラット胚盤胞にマウスES細胞を補完した場合、マウスの細胞が腎臓を補完するという興味深い報告もなされました7)。これらのことからも、異種キメラ動物を用いた胚盤胞補完法では、作れる臓器と作れない臓器があり、しかも、胚盤胞と多能性幹細胞の種の組み合わせによっても作れる臓器、作れない臓器があることが明らかとなりました。
4.胚盤胞補完法で作ることができない臓器がなぜあるのか?
そのため、奈良先端大へ赴任後、まずマウスとラットの異種キメラ動物を作製し、解析することで、『なぜ異種間キメラ動物体内で補完できない臓器があるのか』という問いを明らかにする研究を行いました。その結果、マウスの胚盤胞とマウスES細胞を用いた同種間キメラ動物では、臓器ごとのES細胞由来細胞の寄与率 (キメラ率)は、ほぼ一定であったのに対し、ラットES細胞とマウス胚盤胞を用いた異種間キメラ動物においては、臓器ごとのキメラ率は一定ではなく、ラット細胞は、特にマウスの腎臓へと寄与できず、マウスの胃や肺には寄与しやすいことが分かってきました(図2)。この結果から、腎臓欠損マウス体内でラット腎臓ができない理由は、ラット細胞がマウスの腎臓へほとんど存在できないためである可能性が考えられました。そのため、ラット細胞が比較的寄与しやすい肺であれば、マウス体内で作ることが可能であるのではと次に考えました。まず、肺欠損マウスモデルを作製し、肺の形成のために必要なマウスの野生型細胞数を調べたところ、野生型細胞がキメラ個体におよそ10%以上存在した時、肺が形成されることがわかりました。つまり、同種間の胚盤胞補完法であったしても、野生型の細胞の寄与率が低い場合には、臓器が形成されない場合があることが明らかとなりました。また、ラットの細胞はほとんどの場合、マウスの肺へ10%以上は存在できることがわかっていましたので、肺の欠損マウス胚に対して、ラットのES細胞を注入したところ、ラット由来の肺をマウス体内で作製することに世界的に初めて成功することができました8)(図3)。これらの結果からも、胚盤胞補完法により臓器を作製するためには、臓器形成時に一定の数以上の多能性幹細胞由来の正常細胞が存在することが重要である可能性が示唆されました。
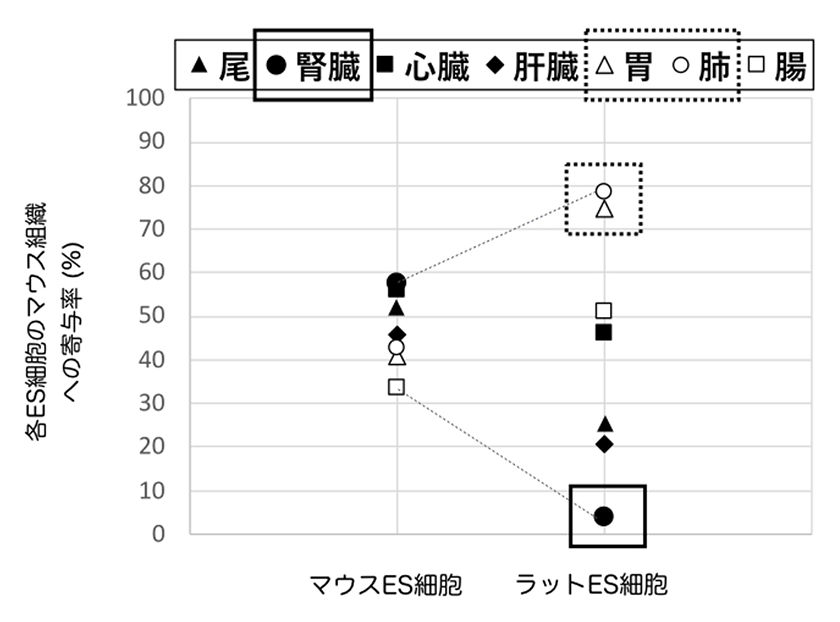
図2.マウス体内におけるマウスES細胞とラットES細胞の組織への寄与率
マウスES細胞は、マウス体内において、各組織への寄与率が比較的一定である。ラットES細胞は、マウス体内において、腎臓、尾、肝臓へは寄与しづらく、肺、胃には寄与しやすい傾向がある。
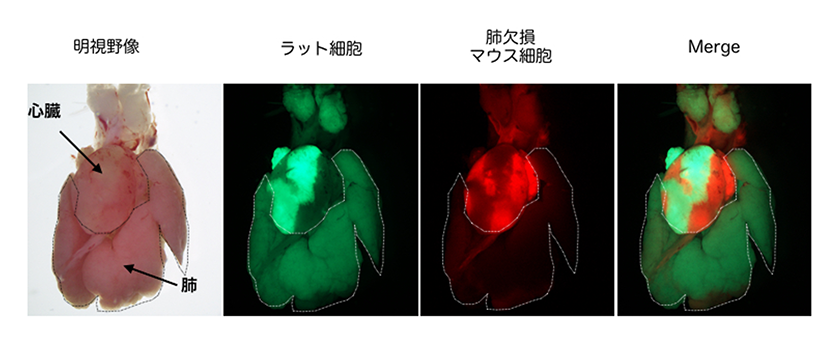
図3.肺欠損マウスモデル胚へラットES細胞を注入して作成されたラット肺
ラットES細胞が寄与するキメラでは、ラット細胞由来の肺(緑)が形成されている。また、肺においてマウス細胞(赤)がほとんど検出されていないことから、肺はほぼラット細胞からのみ構成されていることがわかる。
5.おわりに
これまでの知見から、今後は胚盤胞補完法により臓器を作るためには、それぞれの臓器に対してどの程度の野生型の細胞が寄与する必要があるかを明らかにしていく必要があると考えています。また、現在、ヒト多能性幹細胞とブタなどの異種の臓器欠損モデル動物を用いた胚盤胞補完法を行い、ヒト臓器を異種の動物体内で作り出す研究も進んでいますが、異種動物体内でのヒト臓器の作製は未だ成功が報告されていません9)。これは、ヒト多能性幹細胞を異種であるブタやウシなどの胚盤胞へ注入しても、ヒト由来の細胞はキメラ体内にほとんど寄与できないこと10) が大きな要因であると考えらます。そのため、今後は異種細胞が寄与しにくい臓器に対し、寄与率を高めるにはどうすればよいかという研究を進めていき、最終的には、ヒト臓器を異種動物体内に作製することへと発展させていきたいと考えています。
参考文献
- Takahashi K. et al. (2006) Cell, 126, 663-676.
- Chen J. et al. (1993) Proc Natl Acad Sci U S A 90, 4528-4532.
- Kobayashi T. et al. (2010) Cell.142, 787-799.
- Isotani A. et al. (2012) Genes to Cell 16, 397-405.
- Usui J. et al. (2012) Am J Pathol 180, 2417-2426.
- Hamanaka S. et al. (2018) Stem cell reports 11, 988-997.
- Goto T. et al. (2019) Nat Commun 10,451.
- Yuri S. et al. (2022) Biorxiv.
- Das S. et al. (2020) Nat Biotech, 38, 297-302.
- Wu J. et al. (2017) Cell 168, 473-486.
由利 俊祐 NAIST Edge BIO, 0006. (2022)

