2024.06.11
医薬・化粧品原料を発酵高生産する微生物の分子育種
微生物分子機能学研究室・客員准教授・小暮高久
- 要旨
- 微生物の多様な代謝能力を利用する発酵生産技術は、古くから発酵食品の製造に利用されてきましたが、近年は遺伝子資源の飛躍的増大や人工代謝経路の設計・導入といった合成生物学的手法等の発展により、元来微生物が生産しない物質も含め、様々な有用物質のバイオ生産に展開可能となっています。私たちは、アミノ酸の工業的発酵生産に用いられているコリネ型細菌Corynebacterium glutamicumを利用した有用物質生産菌の開発に取り組んでいます。コリネ型細菌は、高い物質生産能力に加え、毒性物質への高耐性などバイオ生産宿主としての堅牢性を兼ね備えていることがわかってきています。本菌に対して、目的とする化合物の生産性を最大化するための代謝設計に基づいた遺伝子改変を加えることで、バイオ燃料やバイオマスプラスチック原料、医薬・化粧品原料、香料等を含む多様なバイオ化学品を発酵高生産可能な菌株を創出することができます。本稿では、医薬・化粧品やポリマー材料の原料として有用な芳香族関連化合物であるシキミ酸およびプロトカテク酸を糖原料から発酵高生産可能な菌株をそれぞれ分子育種した事例について紹介します。
- 主要関連論文
- Kogure T, Suda M, Hiraga K, Inui M. Protocatechuate overproduction by Corynebacterium glutamicum via simultaneous engineering of native and heterologous biosynthetic pathways. Metab. Eng. (2021) 65: 232-242
DOI: 10.1016/j.ymben.2020.11.007 - Kogure T, Kubota T, Suda M, Hiraga K, Inui M. Metabolic engineering of Corynebacterium glutamicum for shikimate overproduction by growth-arrested cell reaction. Metab. Eng. (2016) 38: 204-216
DOI: 10.1016/j.ymben.2016.08.005.
1.はじめに
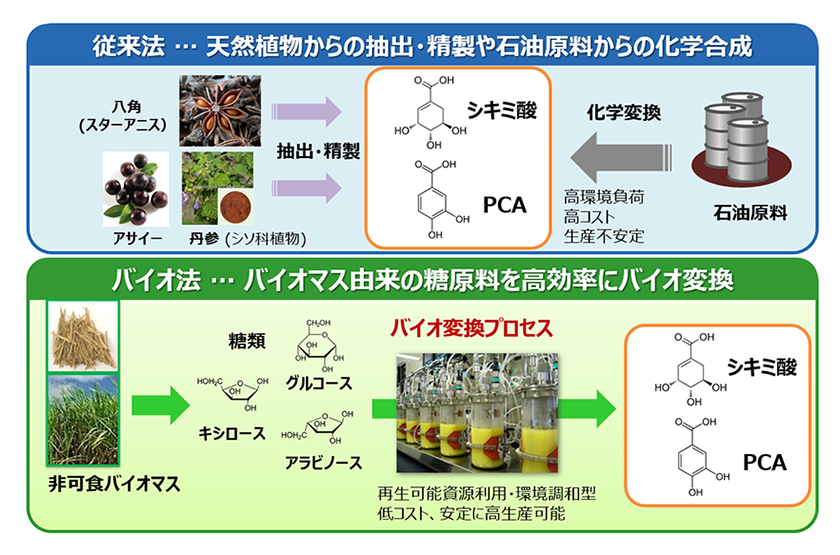
近年、合成生物学の手法を用いて微生物や動植物が保有する多様な代謝変換能力を利用・改変し、再生可能なバイオマス資源を原料として有用化学品を発酵生産させる「バイオものづくり」技術が循環型社会形成の鍵となる技術として注目されています。私たちは、アミノ酸の工業的発酵生産に利用されている有用微生物であるコリネ型細菌を利用した有用物質生産技術の開発に取り組んでいます。本菌は、菌の増殖が抑制される嫌気条件下や栄養成分制限下においても高い代謝能力を維持しており、私たちは、この代謝能力を活用した増殖非依存型の高効率発酵生産プロセスの基盤技術を確立しています1)。本基盤技術をベースとして、さらに生産ターゲットとする化合物の生産能力の付与および生産性向上に関わる遺伝子レベルでの分子育種を適用することで、様々な有用化学品の発酵高生産菌の育種が可能となります2)。本稿では、実用化レベルの生産性を達成しているバイオ化学品として、医薬・化粧品原料やポリマー原料として有用な芳香族関連化合物であるシキミ酸およびプロトカテク酸の高生産菌の開発事例について紹介します3,4)。これらの化合物は特定の植物の果実等に含まれる生理活性物質として知られており、植物からの抽出・精製が主な製造法となっていたことから、高価格で供給量も限定されていました。これらの化学品の発酵高生産技術が確立されたことにより、各化学品を飛躍的に高い生産性で生産し、安定供給することが可能となりました(図1)。
2.シキミ酸生産菌の育種3)
植物や微生物において生産される多種多様な芳香族系化合物は、シキミ酸経路と呼ばれる共通代謝経路を起点として生合成されています。シキミ酸は、この経路の名前の由来となっている環状ヒドロキシ酸であり、インフルエンザ治療薬タミフルの製造原料とされる他、美白や育毛効果、抗炎症作用等、様々な薬理活性を有していることが知られています。シキミ酸は従来、トウシキミという植物の果実(調味料として使われる八角)からの抽出法により製造されていましたが、低収量で供給量も限られるといった問題が存在します。コリネ型細菌もシキミ酸経路においてシキミ酸を生成しますが、野生株ではシキミ酸は代謝変換されて芳香族アミノ酸等の生産に使われるため、蓄積はしません。このため、本菌においてシキミ酸を生産させるためには、シキミ酸の代謝酵素であるシキミ酸キナーゼを遺伝子破壊によって欠損させるか、酵素活性を弱化させることが必要となります(図2)。一方、野生型株においてはシキミ酸経路に流入する代謝フラックスは本経路の初発酵素であるDAHP(中央代謝で生成するホスホエノールピルビン酸(PEP)とエリスロース-4-リン酸(E4P)の縮合により生成するシキミ酸経路の初発化合物)合成酵素の活性制御(芳香族アミノ酸によるフィードバック抑制)により低く抑えられていることから、シキミ酸キナーゼの欠損や活性弱化のみではシキミ酸の高生産には至りません。そこでシキミ酸高生産をもたらす改変の鍵となったのが、酵素活性のフィードバック抑制が解除された変異型DAHP合成酵素の利用でした。私たちは、大腸菌由来の変異型のフィードバック抑制耐性型DAHP合成酵素(AroG(S180F))をコリネ型細菌のシキミ酸キナーゼ欠損株において高発現させることにより、本菌によるシキミ酸生産性が大幅に向上することを確認しました(図2、3)。これらの改変に加え、DAHPからシキミ酸への変換酵素であるAroB, AroD, AroEの発現強化、シキミ酸の前駆体であるE4Pの供給量向上を狙ったペントース・リン酸経路酵素Tkt、Talの発現強化、及び副生経路遺伝子であるQsuBとQsuDの破壊を順次組み合わせることにより、遺伝子改変株のシキミ酸生産能力が段階的に高まることを確認しました(図3)。育種菌株は、ジャーファーメンター制御下での増殖非依存型の菌体反応において、48時間で、141 g/L(対糖モル収率: 51%)ものシキミ酸をグルコースから生産可能であることを確認しました3)。
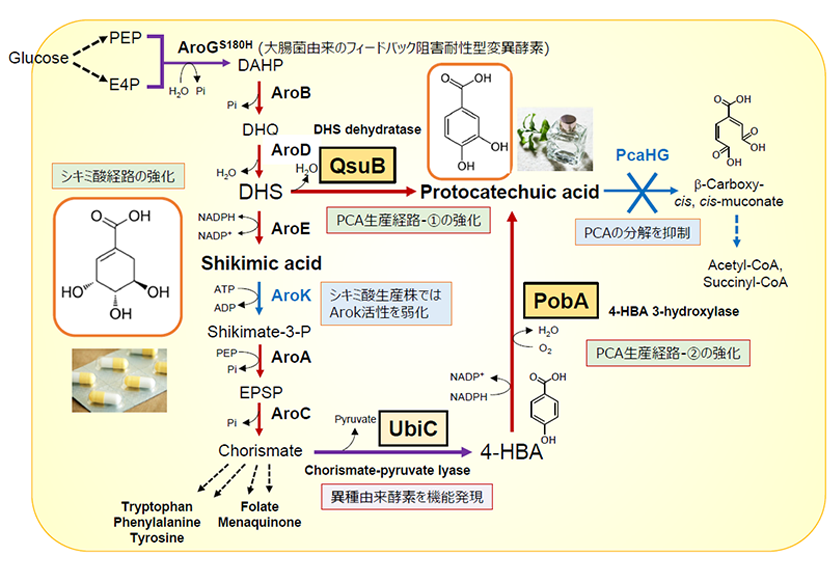
図2.シキミ酸およびプロトカテク酸の生産経路とそれらの高生産に関わる代謝改変
赤色および紫色の矢印は、遺伝子発現を強化した代謝ステップを示す(赤: 内在性遺伝子、紫: 外来遺伝子)。また、青色の矢印(および×印)は、酵素活性を弱化または遺伝子破壊した代謝ステップを示す。
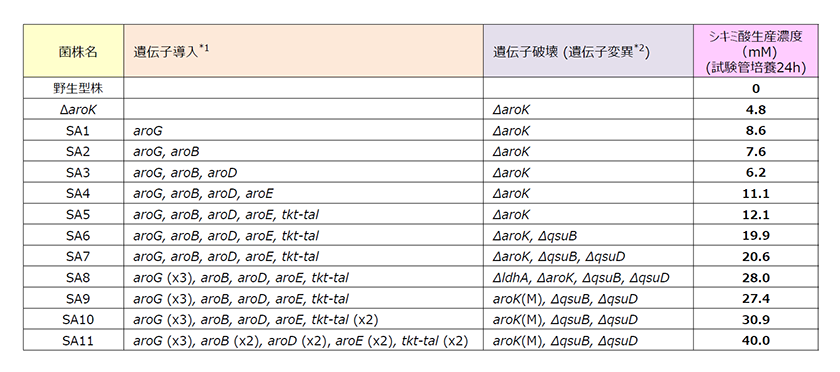
図3.遺伝子改変によるシキミ酸生産性の向上
*1 括弧内の数字は各遺伝子の染色体導入コピー数を示す(記載がない遺伝子の染色体導入コピー数は1コピー)。
*2 aroK(M): 酵素活性が弱化したAroKをコードする遺伝子
3.プロトカテク酸生産菌の育種4)
プロトカテク酸(3, 4-ジヒドロキシ安息香酸、PCA)は、抗菌、抗ウイルス、抗癌、抗炎症、抗動脈硬化等、様々な薬理活性を有していることが報告されており、医薬・化粧品原料として有望な芳香族カルボン酸です6)。PCAはまた、接着剤等のポリマーや香料(バニリン)の原料としての用途も存在します。一方、コリネ型細菌は前述のシキミ酸やキナ酸といった環状ヒドロキシ酸を炭素源として資化可能であり、その資化経路上では、シキミ酸の直前前駆体であるデヒドロシキミ酸(DHS)のPCAへの代謝変換を介して異化代謝が進行します。そこで、PCA生成に関わる内在性酵素であるDHSデヒドラターゼ(QsuB)を高発現させて活性強化するとともに、PCAの異化代謝に関わる酵素(PcaHG)を遺伝子破壊して欠損させることにより、糖からのPCA生産が可能となります(図2)。一方、コリスミ酸の4-ヒドロキシ安息香酸 (4-HBA)への変換を触媒する酵素であるコリスメートピルベートリアーゼ(UbiC、コリネ型細菌は保有していない)を機能発現させることで、シキミ酸経路の最終ステップで生成するコリスミ酸からもPCA生成が可能となります。即ち、高活性酵素として見出したProvidencia rustigianii由来のUbiCをコリネ菌において機能発現させることによりコリスミ酸を4-HBAに変換させると5)、内在性の4-HBA-3-ヒドロキシラーゼ活性によって4-HBAの芳香環の3位が水酸化されることでPCAが生成します(図2)。これら2種のPCA生成ルートの構成遺伝子をすべて強力なgapAプロモーター制御下で高発現させることで両経路を強化した菌株を構築し、ジャーファーメンター制御による菌体反応を行った結果、グルコースから83 g/L(対糖モル収率: 33%)のPCAが32時間で生産されました4)。生産物であるPCAは強い細胞毒性を示すことから、高濃度のPCAは菌の増殖・代謝や発酵生産を阻害する可能性も考えられましたが、コリネ型細菌が保持する毒性化合物に対する高耐性によって発酵阻害が回避され、高濃度のPCA生産を可能としたと考えられます。
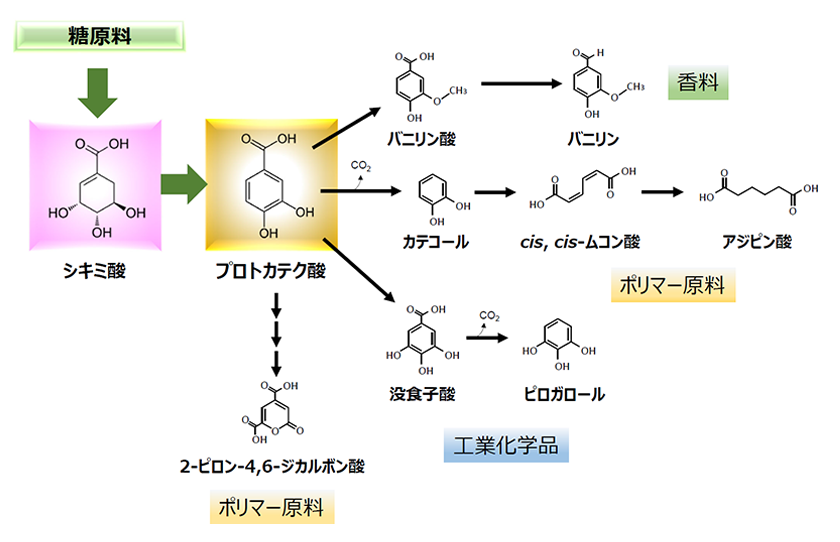
PCAはまた、カテコール、香料のバニリン、バイオポリマー原料となるcis, cis-ムコン酸等のバイオ生産経路における共通前駆体でもあることから、PCA高生産株をベースとした、それら有用化学品の高生産菌育種への展開が可能となりました(図4)。
4.終わりに
微生物を利用した発酵法による有用化学品のバイオ生産技術は、医薬・化粧品、香料、機能性栄養素材、ポリマー材料等、幅広い用途のある様々な化学品を高効率かつ再生可能資源からカーボンニュートラルに生産可能な環境調和型技術といえます。近年は、発展が著しいAI・デジタル技術を融合させた合成生物学的手法やマルチオミクス解析技術、代謝解析や菌株構築を自動化するロボティクス技術等を適用した有用物質生産菌の開発が国内外で活発化しています。今後は、バイオ生産可能な物質のさらなる多様化に加え、非可食バイオマスや食品廃棄物、さらには廃棄衣料等の未利用資源を原料として有用化学品を生産する「バイオアップサイクル」技術の開発の進展が期待されています。当該技術は、石油資源依存からの脱却とサーキュラーエコノミー(循環型経済)の形成に大きく寄与することが期待されます。
参考文献
- Jojima, T., Inui, M., Yukawa, H., Springer-Verlag Berlin Heidelberg, pp. 149-172.(2013)
- Kogure T. and Inui, M., Appl Microbiol Biotechnol. 102:8685-8705. (2018)
- Kogure T. et.al., Metab. Eng. 38: 204-216.(2016)
- Kogure T, et.al., Metab. Eng. 65: 232-242.(2021)
- Kitade Y, et.al., Appl. Environ. Microbiol. 84(6) (2018)
- Kakkar, S., Bais, S., ISRN Pharmacol. 952943 (2014)
小暮 高久 NAIST Edge BIO, 0025. (2024)