神経細胞が正しい経路に沿って軸索を伸ばす仕組みを解明
~ガイダンス分子と軸索上の受容体の“接着”を利用した 進路決定機構が明らかに~
脳疾患の解明や再生医療への応用に期待
神経細胞が正しい経路に沿って軸索を伸ばす仕組みを解明
~ガイダンス分子と軸索上の受容体の“接着”を利用した 進路決定機構が明らかに~
脳疾患の解明や再生医療への応用に期待
【概要】
奈良先端科学技術大学院大学(学長:塩﨑 一裕)先端科学技術研究科 バイオサイエンス領域 神経システム生物学研究室 博士後期課程 3 年のQiu Zhen(キュウ シン)、嶺岸卓徳助教、稲垣直之教授らのグループは、神経細胞の軸索(注1)が伸長するときに、細胞外環境に存在する軸索ガイダンス分子と軸索にある受容体の接着を利用して軸索の進行方向を決定することを明らかにしました。また、この仕組みが働かなくなると、軸索が正しい方向に伸びなくなることも突き止めました。
わたしたちの脳内では、神経細胞が軸索と呼ばれる長い突起を正しい経路に沿って伸ばし、標的の神経細胞と結合することで脳の活動に必要な神経ネットワークを形成します。この過程では、軸索の先端が細胞の外に存在するガイダンス分子を検知して、軸索の進路を決定します。代表的な誘引性軸索ガイダンス分子であるネトリン(注2)は、細胞外環境に拡散して存在し、長距離にわたって適切な方向に軸索を誘引することが広く知られています。最近になり、ネトリンが細胞の道路に相当する細胞外環境(細胞外基質)に結合し、軸索が路面上のネトリンに誘引されて伸びることがわかってきました。しかし、軸索がどのようにしてネトリンの路面に沿って伸びるのか、その仕組みはよくわかっていませんでした。
今回の研究で、稲垣教授らは、ネトリンの受容体タンパク質DCCが自動車のタイヤのように路面上のネトリンと“グリップ”して軸索の先端を動かす推進力を生み出したり、路面をスリップして推進力を弱めたりすることで進行方向や速度を調節する仕組みを解明しました。また、この仕組みが働かなくなると、軸索がネトリンの路面に沿って正しく伸ばすことができなくなることもわかりました。
本研究の成果により神経ネットワーク形成やヒトの脳疾患についての理解が深まるとともに、再生医療への応用などが期待できます。
本研究成果は、国際科学雑誌Frontiers in Molecular Neuroscience に 2024 年 2 月 5 日(月)に公開されました(DOI:10.3389/fnmol.2024.1307755)。
【背景と目的】
脳内の神経細胞は、軸索を正しい経路に沿って伸ばし、標的の神経細胞と結合することで脳の活動に必要な神経ネットワークを形成します。その方法としては、軸索の先端が周囲を拡散するガイダンス分子の濃度差を感知し、誘引分子が多い方向に軸索を伸ばす走化性と、軸索の先端が細胞外基質に結合したガイダンス分子に直接接触し、探索しながら軸索を伸ばす走触性によって制御されることが知られています。代表的な軸索ガイダンス分子であるネトリンは、走化性因子として長距離にわたって軸索を誘引することが知られていましたが、最近になり走触性因子として軸索を短距離誘引することもわかってきました。ネトリンを介した走触性には、その受容体であるDCCが重要な役割を果たすことが報告されていましたが、軸索がどのようにして細胞外基質上のネトリンに誘引されるのか、その仕組みはわかっていませんでした。稲垣直之教授らのグループは、これまでの研究で、シューティン(注3)という分子が、軸索先端でエンジンの役割を果たすアクチン線維とタイヤの役割を果たす細胞接着分子を連結(クラッチ)することによって軸索を伸ばすための力を生み出すことを報告していました。
今回、研究グループは、軸索の先端でシューティンがアクチン線維とDCCを連結することを見出しました。さらに、軸索の先端が細胞外基質上のネトリンを検知して軸索の進行方向を決定する仕組みを調べました。
【研究の内容】
実験では、マウス脳内の海馬という組織にある神経細胞を培養し、材料として使用しました。神経細胞は、軸索ガイダンス分子のネトリンとポリリジン(コントロール基質)のマイクロパターン(注4) をコーティングした細胞外基質上に培養しました。本研究において軸索先端上のDCCの動きを、高感度顕微鏡カメラと全反射顕微鏡を用いてライブ計測しました。さらに、軸索の先端で発生する微細な推進力の測定のために、神経細胞を複数の蛍光ナノビーズ(ゲルの変形をモニターする粒子)を包埋したゲルの上に培養し、力の発生に伴うゲルの歪みをビーズの動きから計測しました。発生した駆動力の大きさと方向は、計測したビーズの動きをコンピューターで解析して求めました。
【結果】
神経細胞をネトリンとポリリジンのマイクロパターン上で培養すると、ネトリンに沿って軸索を伸ばすことがわかりました。しかし、シューティンノックアウト(シューティンの欠失)によりアクチン線維とDCCの連結を切ると、軸索はネトリンに沿って伸ばすことができなくなりました。この結果から、ネトリンに向かう軸索の走触性には、アクチン線維(エンジン)がシューティン(クラッチ)を介してDCC(タイヤ)と連結することが必要であることがわかりました(図 1)。また、ネトリン上では、軸索先端のDCCが路面をしっかり捉えて(グリップして)推進力を効率的に生み出す一方、ポリリジン上ではDCCがスリップして推進力が効率的に路面に伝わらないことがわかりました。以上の結果から、軸索先端がDCCと路面とのグリップとスリップを巧妙に利用して正しい方向に進んでゆくことが明らかとなりました(図 1)。
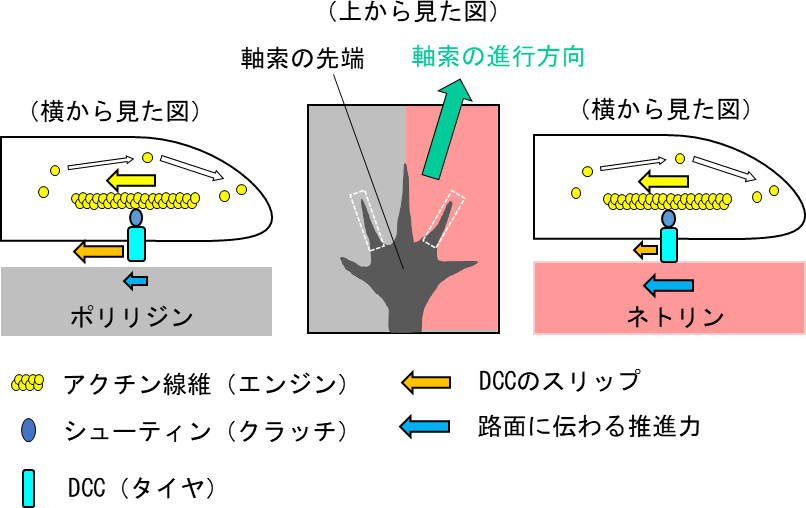
軸索先端がネトリンとポリリジンの境界上にある場合、ラミニン上ではDCCが路面をしっかり捉えて(グリップして)推進力を効率的に生み出す(青矢印)。一方、ポリリジン上ではDCCが大きくスリップ(黄矢印)をして推進力が効率的に路面に伝わらない。その結果、軸索先端に接する路面に方向性を持った推進力が生じて軸索の進行方向が決定される(緑矢印)。
【今後の展開】
今回の研究は、ネトリンによる軸索の走触性の仕組みを分子と力のレベルで明らかにした点に意義があります。これまで、ネトリンは軸索先端のDCCに結合して細胞内シグナル伝達を起こし、軸索の伸長を誘引すると考えられていました。一方、本研究は、DCCが細胞外基質上でネトリンに対する細胞接着分子として働くことで、細胞内シグナル伝達には依存せずに軸索の走触性を起こすことを明らかにしました。軸索を適切な場所に伸ばす分子の仕組みの解明は、神経再生の治療法開発にとって基盤となる知見となります。今回の研究成果は、神経科学に加えて医学領域の研究の加速も期待できます。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「細胞-基質間の力を基盤とした細胞移動と神経回路形成機構の解明およびその破綻による病態の解明」(研究開発代表者:稲垣 直之)および日本学術振興会(JSPS)科学研究費、大阪難病研究財団による支援によって実施しました。
【用語解説】
(注1)軸索:神経細胞から伸びる長い突起。他の神経細胞と結合することで脳の活動に必要な情報ネットワークを作る。神経細胞のシグナルは、軸索を通して他の細胞に伝えられる。発生時期の神経ネットワーク形成の過程では、軸索の先端が外部環境を探索しながら正しい方向へと進んでゆく。
(注2)ネトリン:神経軸索を誘引する分子の一つ。軸索の誘引のみならず乳腺や肺、血管の形成にも関与することが知られている。
(注 3)シューティン:脳に存在するタンパク質で、これまでの研究から、神経ネットワーク形成に関
わる軸索伸長の方向決定(軸索ガイダンス)や、神経細胞の移動などに関わることが知られている。
(注4)マイクロパターン:本実験のネトリンとポリリジンのマイクロパターンの作成法として、ガラスをポリリジンでコートし、その上に幅14 マイクロメートルのネトリンでコートされた道筋を作った。
【掲載論文】
タイトル:Adhesion-Clutch between DCC and Netrin-1 Mediates Netrin-1–induced Axonal Haptotaxis
著 者 :Zhen Qiu, Takunori Minegishi, Daichi Aoki, Kouki Abe, Kentarou Baba, and Naoyuki Inagaki
掲載誌:Frontiers in Molecular Neuroscience
DOI:10.3389/fnmol.2024.1307755
【神経システム生物学研究室】
研究室紹介ページ:https://bsw3.naist.jp/courses/courses204.html
研究室ホームページ:https://bsw3.naist.jp/inagaki/
(2024年02月07日掲載)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学